ESTRUCTURA Y FUNCIÓN DE LA MEMBRANA
PLASMÁTICA
Las paredes externas de una
casa o un automóvil proporcionan una barrera sólida e inflexible que protege a
las personas de un mundo exterior impredecible y violento. Podría esperarse que
el límite externo de una célula viva se construyera con una barrera igual de
resistente e impenetrable porque también debe proteger su delicado contenido
interno de un ambiente inerte y a menudo inhóspito. Aun así, las células están
separadas del mundo exterior por una estructura delgada y frágil llamada membrana
plasmática, que sólo mide 5 a 10 nm de espesor. Se necesitarían cerca de cinco
mil membranas plasmáticas una sobre otra para igualar el grosor de una sola página
de este libro.
Como es tan delgada, no se
encuentra ningún indicio de la membrana plasmática cuando se examina una
preparación celular con el microscopio óptico. De hecho, fue hasta finales del
decenio de 1950, cuando las técnicas para preparar y teñir el tejido progresaron,
y la membrana plasmática pudo analizarse con el microscopio electrónico. Estas
micrografías electrónicas iniciales, como las tomadas por J. D. Robertson de la
Duke University, presentaron a la membrana plasmática como una estructura de
tres capas, consistente en dos capas externas teñidas de color oscuro y una capa
intermedia clara. Todas las membranas que se examinaron de cerca, ya fueran
plasmáticas, nucleares o citoplásmicas, tomadas de plantas, animales o
microorganismos, mostraron la misma ultraestructura. Además de suministrar una
imagen visual de esta estructura celular vital, estas micrografías electrónicas
iniciaron un fuerte debate sobre la composición de la membrana, un argumento que llegó al corazón
mismo del tema de la estructura y función de la membrana. Como se verá después,
las membranas celulares contienen una capa doble de lípidos, y las dos capas
con tinción oscura en las micrografías electrónicas de la corresponden a las
superficies polares interna y externa de la bicapa. Más adelante se regresará a
la estructura de las membranas, pero primero se revisan algunas de las
principales funciones de las membranas en la vida de una célula.
Las membranas plasmáticas son estructuras
muy delgadas y delicadas, pero tienen un papel clave en muchas de las funciones
más importantes de las células.
La membrana plasmática
separa a la célula viva de su ambiente; constituye una barrera de permeabilidad
selectiva que permite el intercambio de ciertas sustancias al tiempo que
previene el paso de otras; contiene los mecanismos para transportar las
sustancias de un lado al otro de la membrana; aloja los receptores que se unen con
ligando específicos en el espacio externo y transmiten información a los
compartimientos internos de la célula; media las interacciones con otras
células; proporciona un marco en el que pueden organizarse los componentes; es
un sitio en el que la energía se traduce de un tipo a otro.
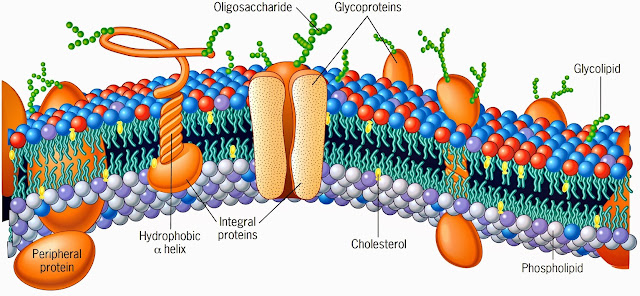
Las membranas son estructuras de lípidos
y proteínas en las que los componentes se mantienen unidos en una hoja delgada
mediante enlaces no covalentes.
La membrana se mantiene
unida como una hoja cohesiva por una bicapa de lípidos consistente en una capa
bimolecular de lípidos anfi páticos, cuyos grupos cabeza polares se dirigen hacia
fuera y las colas acilo grasas hidrófobas se dirigen hacia el interior. Entre
los lípidos se incluyen fosfoglicéridos como la fosfatidilcolina; lípidos con
base de esfi ngosina como el fosfolípido esfingomielina, y los cerebrósidos y
gangliósidos que contienen carbohidratos (glucolípidos), además de colesterol. Las proteínas de la
membrana pueden dividirse en tres grupos: proteínas integrales que penetran en
y a través de la bicapa lipídica, con porciones expuestas en las superficies
citoplásmica y extracelular de la membrana; proteínas periféricas que se
localizan completas fuera de la bicapa de lípidos pero no tienen enlaces
covalentes con los grupos cabeza polares de la bicapa de lípidos ni con la
superficie de una proteína integral, y proteínas fi jadas por lípidos que están
fuera de la bicapa lipídica, pero tienen enlaces covalentes con lípidos que
forman parte de la bicapa. Los segmentos transmembranosos de las proteínas
integrales casi siempre se encuentran como una hélice alfa, compuesta sobre
todo por residuos hidrófobos.
Las membranas son estructuras muy
asimétricas cuyas dos hojas tienen propiedades muy diferentes.
Como ejemplos, todas las
cadenas de carbohidrato de la membrana se dirigen en sentido contrario al citosol;
muchas de las proteínas integrales tienen sitios en su superficie externa que
interactúan con ligandos extracelulares y sitios en su superficie interna que
interactúan con proteínas periféricas y forman parte de un esqueleto de la
membrana interna; además, el contenido de fosfolípidos de las dos mitades de la
bicapa es muy asimétrico. La mejor forma de revelar la organización de las
proteínas dentro de la membrana es en réplicas congeladas y fracturadas en las que
se congelan las células, se dividen sus membranas por el centro de la bicapa
por un plano de fractura y se visualizan las caras internas expuestas mediante
la formación de una réplica en metal.
El estado físico de la bicapa lipídica tiene
importantes consecuencias para la movilidad lateral de los fosfolípidos y las
proteínas integrales.
La viscosidad de la bicapa y
la temperatura en la cual sufre la transición de fase dependen del grado de
insaturación y la longitud de las cadenas acilo grasas de los fosfolípidos. El
mantenimiento de una membrana fluida es importante para muchas actividades
celulares, como la transducción de señales, división celular y formación de regiones
especializadas de membrana. Al principio, la difusión lateral de las proteínas
dentro de la membrana se demostró por fusión celular y puede cuantificarse con
técnicas que siguen los movimientos de las proteínas marcadas con compuestos fluorescentes
o marcadores electrodensos.
La medición de los coeficientes
de difusión de las proteínas integrales sugiere que la mayoría está sujeta a
infl uencias restrictivas que inhiben su movilidad. Las proteínas pueden estar
limitadas por su relación con otras proteínas integrales o con proteínas
periféricas localizadas en la superficie de la membrana. A causa de estos
diversos tipos de restricciones, las membranas alcanzan una considerable medida
de estabilidad organizacional en la que se diferencian entre sí las regiones particulares
de membrana
La membrana plasmática del eritrocito contiene
dos proteínas integrales principales, la banda 3 y la glucoforina A, así como
un esqueleto interno bien definido compuesto de proteínas periféricas.
Cada subunidad de banda 3
abarca toda la membrana por lo menos una docena de veces y contiene un canal
interno por el cual se intercambian aniones bicarbonato y cloro. La glucoforina
A es una proteína muy glucosilada con función incierta que contiene un solo dominio
transmembranoso consistente en una hélice alfa hidrófoba. El principal
componente del esqueleto de la membrana es la proteína fi brosa espectrina, que
interactúa con otras proteínas periféricas para suministrar soporte a la
membrana y limitar la difusión de sus proteínas integrales.
La membrana plasmática es una barrera con
permeabilidad selectiva que permite el paso de solutos por varios mecanismos,
entre ellos la difusión simple a través de la bicapa lipídica o canales en la
membrana, difusión facilitada y transporte activo.
La difusión es un proceso independiente
de energía donde un soluto se mueve en favor de un gradiente electroquímico, lo
que disipa la energía libre almacenada en el gradiente. Los solutos inorgánicos
pequeños, como el O2, CO2 y H2O, penetran con facilidad la bicapa de lípidos,
al igual que los solutos con coeficientes de partición altos (alta solubilidad
en lípidos). Los iones y los solutos orgánicos polares, como los azúcares y los
aminoácidos, requieren transportadores especiales para entrar o salir de la
célula.
El agua se mueve por ósmosis a través de
la membrana plasmática semipermeable de una región con menor concentración de
solutos (el compartimiento hipotónico) a una región con mayor concentración de
soluto (el compartimiento hipertónico).
La ósmosis tiene un papel
clave en múltiples funciones celulares. Por ejemplo, en las plantas la entrada
de agua genera presión de turgencia contra la pared celular que ayuda a
sostener los tejidos no leñosos
Los iones se difunden a través de la
membrana plasmática mediante canales especiales recubiertos con proteína que a
menudo son específicos para iones particulares.
Los canales iónicos casi
siempre tienenvuna compuerta que se controla por voltaje o ligandos químicos, como
los neurotransmisores. El análisis de un canal iónico bacteriano (KcsA) reveló
cómo los átomos de oxígeno que fl uyen de la columna vertebral del polipéptido
son capaces de sustituir a las moléculas de agua que habitualmente se
relacionan con iones K+, lo que permite que la proteína conduzca en forma
selectiva iones K+ a través de su canal central. Los canales de K+ activados por
voltaje contienen un segmento helicoidal cargado que se mueve como respuesta al
voltaje de la membrana, lo cual abre o cierra la compuerta.
La difusión facilitada y el transporte activo
requieren la participación de las proteínas integrales de la membrana que se
combinan en forma específica con el soluto que se transporta.
Los transportadores
facilitadores actúan sin gasto de energía y mueven
solutos en favor del
gradiente de concentración en ambas direcciones a través de la membrana. Se
cree que actúan mediante el cambio en la conformación, lo cual expone el sitio de
unión con soluto a ambos lados de la membrana en forma alternada. El
transportador de glucosa es un transportador facilitador cuya presencia en la
membrana plasmática se estimula por los niveles altos de insulina. Los
transportadores activos requieren el gasto de energía y mueven iones y solutos
en contra del gradiente de concentración. Los transportadores activos tipo P,
como la ATP-asa de Na+/K+, funcionan con el impulso de la transferencia de un
grupo fosfato del ATP al transportador, lo que cambia su afinidad por el ion
transportado. Los sistemas de transporte activo secundario derivan la energía
almacenada en un gradiente iónico para transportar un segundo soluto contra un
gradiente de concentración. Por ejemplo, el transporte activo de la glucosa a
través de la superficie apical de la célula epitelial intestinal se impulsa por
el cotransporte de Na+ en favor de su gradiente electroquímico.
El potencial de reposo a través de la
membrana plasmática se debe sobre todo a la permeabilidad limitada de la
membrana al K+ y está sujeta a cambios drásticos.
El potencial de reposo de
una célula nerviosa o muscular típica es cercano a –70 mV (interior negativo).
Cuando la membrana de una célula excitable se despolariza más allá del valor umbral,
se inician los fenómenos que conducen a la abertura de los canales del Na+ y la
entrada de sodio, lo cual se mide como una inversión en el voltaje a través de
la membrana. Unos milisegundos después de abrirse, las compuertas para el Na+
se cierran y los canales del potasio se abren, lo cual posibilita la salida de
K+ con la restauración del potencial de reposo. La serie de cambios drásticos
en el potencial de membrana después de la despolarización constituye un
potencial de acción.
Una vez que el potencial de acción se
inició, se propaga por sí mismo.
Los potenciales de acción se
propagan porque la despolarización que acompaña al potencial de acción en un
sitio de la membrana es suficiente para despolarizar la membrana adyacente, lo
cual inicia un potencial de acción en ese sitio. En un axón mielinizado, un
potencial de acción en un nodo de la vaina puede despolarizar la membrana del
siguiente nodo, lo que permite que el potencial de acción salte con rapidez de
un nodo a otro. Cuando el potencial de acción llega a los botones terminales de
un axón, se abren las compuertas de calcio en la membrana plasmática, lo que
permite la entrada de Ca2+, que inicia la fusión de las membranas de las
vesículas secretoras que contienen los neurotransmisores con la membrana
plasmática suprayacente. El neurotransmisor se difunde a través de la hendidura
sináptica y se une con los receptores de la membrana postsináptica, lo que
induce despolarización o hiperpolarización de la célula blanco.
PARA COMPLEMENTAR TE RECOMENDAMOS VER LA PARTE 2 DE MEMBRANA CELULAR, EN LA QUE DIDACTICOS VIDEOS AYUDARAN A COMPRENDER MEJOR EL TEMA.





0 comentarios